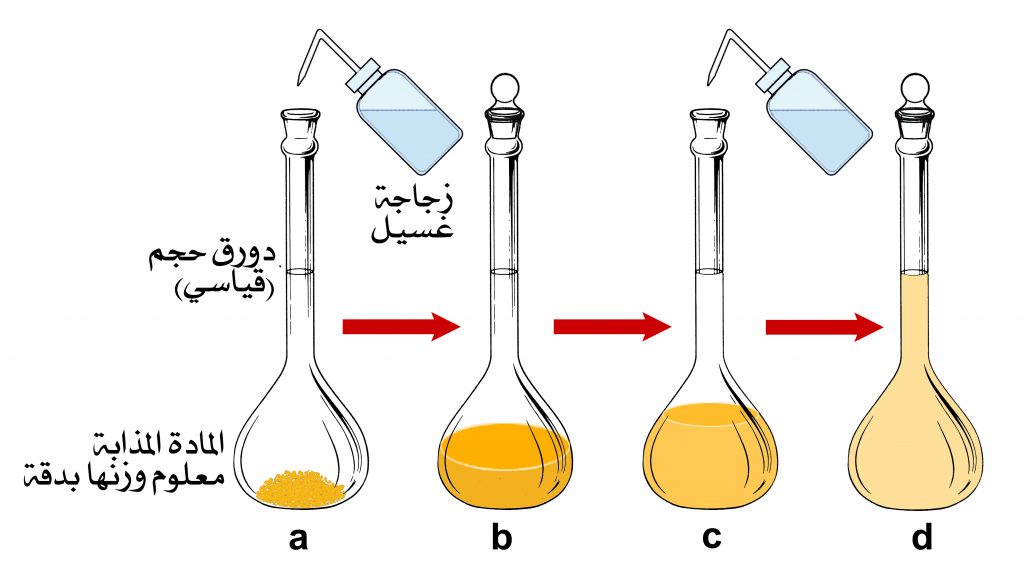
#ثريد من أساسيات الكيمياء العملية : طرق تحضير المحاليل القياسية ⚗️💚.
#معلومات_كيميائية #أثبت_أنك_كيميائي
#معلومات_كيميائية #أثبت_أنك_كيميائي
ماهي المحاليل القياسية؟
من المهم تذكر ان المحلول عبارة عن ( مذاب + مذيب) ولذا فإنه محلول كيميائي يحتوي على تركيز محدد ومعلوم من مادة معينة، ولتحضيره يتم إذابة تركيز محدد من المادة المذابة في المادة المذيبة وغالبا ماتكون (ماء)، حيث يقاس تركيز المحلول بوحدة المولارية (mol/L)
من المهم تذكر ان المحلول عبارة عن ( مذاب + مذيب) ولذا فإنه محلول كيميائي يحتوي على تركيز محدد ومعلوم من مادة معينة، ولتحضيره يتم إذابة تركيز محدد من المادة المذابة في المادة المذيبة وغالبا ماتكون (ماء)، حيث يقاس تركيز المحلول بوحدة المولارية (mol/L)
صممت ملخص مبسّط للطريقة الاولى اتمنى يفيدكم 💚.
drive.google.com
drive.google.com
ايضا هناك طريقة اخرى وهي التخفيف :
باستخدام قانون التخفيف M1V1=M2V2
ويتم فيه تخفيف المحلول الأكثر تركيزا (المحلول الأصلي) للحصول على المحلول المراد تحضيره 🧪
حيث نحصل على الحجم المطلوب أخذه من المحلول الأصلي لتحضير المحلول الجديد ونكمل ماتبقى بالماء الى الحجم المطلوب
باستخدام قانون التخفيف M1V1=M2V2
ويتم فيه تخفيف المحلول الأكثر تركيزا (المحلول الأصلي) للحصول على المحلول المراد تحضيره 🧪
حيث نحصل على الحجم المطلوب أخذه من المحلول الأصلي لتحضير المحلول الجديد ونكمل ماتبقى بالماء الى الحجم المطلوب
سؤال للكيميائين الشُطار👏🏻👩🏻🔬👨🏻🔬
اذا اردت تحضير لمادة NaOH محلول قياسي بسعة 500ml وتركيز 2M، كم الكتلة اللازمة لتحضيره؟
اذا اردت تحضير لمادة NaOH محلول قياسي بسعة 500ml وتركيز 2M، كم الكتلة اللازمة لتحضيره؟
جاري تحميل الاقتراحات...