٨
- ترتبط طاقة المدار بحجمه. كلما قلت الطاقة، صغر المدار.
- تستقر الإلكترونات في المدارات، وتنتقل بين المدارات عند اكتساب أو فقدان الطاقة.
- عند اكتساب الطاقة، تتحرك الإلكترونات إلى مدار أبعد من النواة، والعكس عند فقدان الطاقة، حيث تتحرك الإلكترونات إلى مدار أقرب من النواة.
- ترتبط طاقة المدار بحجمه. كلما قلت الطاقة، صغر المدار.
- تستقر الإلكترونات في المدارات، وتنتقل بين المدارات عند اكتساب أو فقدان الطاقة.
- عند اكتساب الطاقة، تتحرك الإلكترونات إلى مدار أبعد من النواة، والعكس عند فقدان الطاقة، حيث تتحرك الإلكترونات إلى مدار أقرب من النواة.
١٠
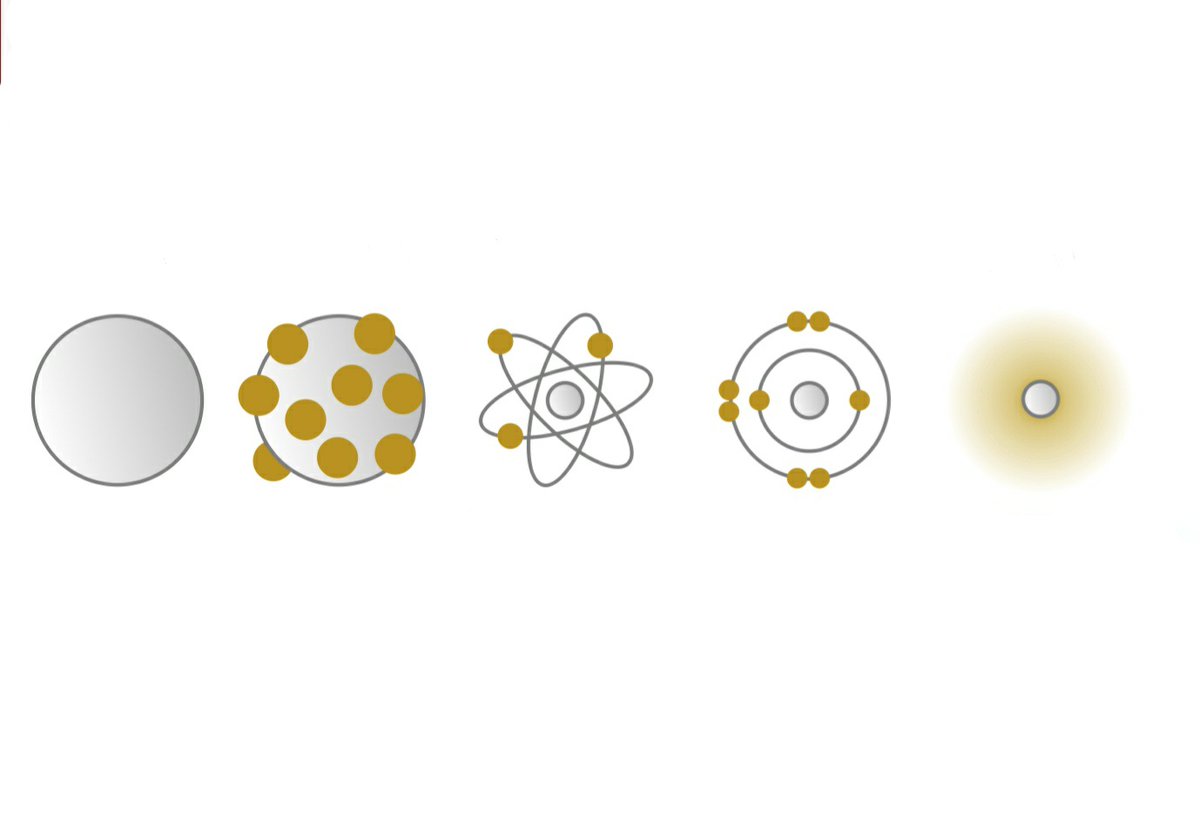
نموذج شرودنغر للذرة
- لا تتحرك الإلكترونات حول النواة في مدارات، بل توجد في مستويات طاقة معينة على شكل سحابة.
- يمكننا أن نتوقع موقع الإلكترون لكن لا يمكننا أن تحديد موقعه على وجه اليقين.
- يساعدنا المدار على التنبؤ بالمنطقة التي يمكننا أن نجد فيها الإلكترون.
نموذج شرودنغر للذرة
- لا تتحرك الإلكترونات حول النواة في مدارات، بل توجد في مستويات طاقة معينة على شكل سحابة.
- يمكننا أن نتوقع موقع الإلكترون لكن لا يمكننا أن تحديد موقعه على وجه اليقين.
- يساعدنا المدار على التنبؤ بالمنطقة التي يمكننا أن نجد فيها الإلكترون.
كل تطوّر بدأ بطرح سؤال ومحاولة البحث الإجابة، حتى لو لم تكن الإجابة صحيحة تمامًا إلا أنها كانت خطوة أساسية لما جاء بعدها. ولهذا يقال: "في العلم، يمكن أن تكون النظرية الخاطئة ذات قيمة وأفضل من عدم وجود نظرية على الإطلاق!"
*** تمت ***
*** تمت ***
جاري تحميل الاقتراحات...